温馨提示: 药品包装不定期更新,请以交付实物为准;为保障用药安全,请严格遵守医嘱或说明书。
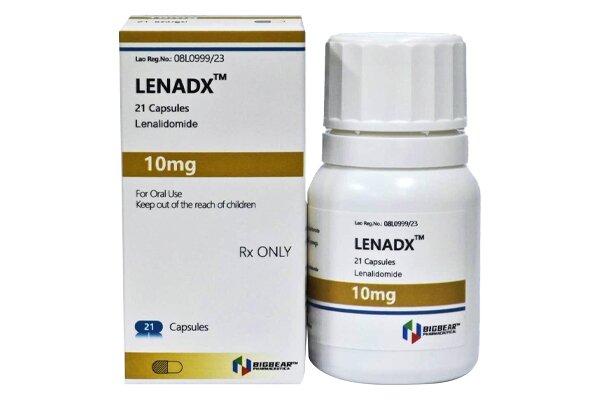
来那度胺 (Lenalidomide,Lenadx)
来那度胺(Lenalidomide)是全球首个口服免疫调节。三重机制,精准打击肿瘤,重塑免疫微环境,是多发性骨髓瘤的持久守护者。
所有称呼来那度胺,Lenalidomide,瑞复美,Revlimid,Lenadx
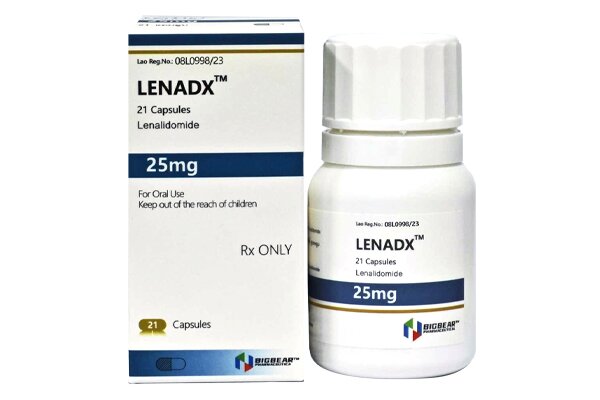
药品规格
- 10mg*21粒/盒
- 25mg*21粒/盒
1、请添加医学顾问,确定无误后,再下单。
2、因药品的特殊性,除质量问题外,恕不退换。
3、服药后有不良反应,不属于药品质量问题。
 微信号
微信号 微信号
微信号
 药厂直销
药厂直销 品质保障
品质保障 全球闪送
全球闪送 隐私保护
隐私保护来那度胺药品新闻
相关栏目
FDA批准来那度胺(Lenalidomide)纳入新诊断多发性骨髓瘤的一线治疗
2015年2月18日,新基公司宣布美国食品药品监督管理局(FDA)已扩大来那度胺(Lenalidomide)联合地塞米松的适应症,纳入新诊断的多发性骨髓瘤患者。该联合方案先前于2006···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:90
FDA批准来那度胺(Lenalidomide)用于复发或难治性套细胞淋巴瘤
2013年6月5日,新基公司宣布美国食品药品监督管理局批准了来那度胺(Lenalidomide)的补充新药申请。该批准 specifically 指定来那度胺(Lenalidomide···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:84
FDA批准Darzalex联合来那度胺(Lenalidomide)用于既往治疗后的多发性骨髓瘤患者
2016年11月21日,杨森生物技术公司宣布,美国食品药品监督管理局已批准Darzalex(达雷妥尤单抗)联合两种标准治疗方案:来那度胺联合地塞米松,或硼替佐米联合地塞米松。该批准 s···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:85
FDA批准来那度胺(Lenalidomide)纳入多发性骨髓瘤自体干细胞移植后的维持治疗
2017年2月22日,新基公司宣布美国食品药品监督管理局(FDA)已扩大来那度胺(Lenalidomide)10毫克胶囊的适应症。这一监管里程碑使来那度胺(Lenalidomide)成···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:84
FDA批准达雷妥尤单抗(Darzalex)联合来那度胺(Lenalidomide)用于新诊断、不适合移植的多发性骨髓瘤
2019年6月27日,强生旗下杨森制药公司宣布,美国食品药品监督管理局(FDA)批准雷妥尤单抗(Darzalex)联合来那度胺和地塞米松(Rd方案),用于新诊断的不适合自体干细胞移植···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:84
FDA批准维布妥昔单抗(Adcetris)联合来那度胺(Lenalidomide)用于复发/难治性弥漫大B细胞淋巴瘤
2025年2月12日,辉瑞公司宣布,美国食品药品监督管理局已正式批准Adcetris®(维布妥昔单抗)的补充生物制剂许可申请。该批准授权维布妥昔单抗(Adcetris)联合来那度胺和一···【更多】
发布时间:2026-03-19文章来源:大熊制药推荐指数:87